Algunas enzimas requieren una coenzima mineral o uno o más iones metálicos para su actividad.
Las enzimas son los catalizadores de las reacciones en los sistemas biológicos así como las proteínas más especializadas, a excepción de un pequeño grupo de moléculas de RNA catalítico que no son proteínas.
Su poder catalítico es a menudo muy superior a los catalizadores sintéticos y actúan en secuencias organizadas catalizando cientos de reacciones consecutivas en las rutas metabólicas mediante las que se degradan nutrientes, se conserva y transforma la energía, y se fabrican macromoléculas biológicas a partir de precursores más sencillos.
Historia de las enzimas
Siglo XIX. La actividad de las enzimas fue descrita por primera vez a principios del siglo XIX, en estudios sobre la digestión de la carne por secreciones del estómago y por la conversión del almidón en azúcar por la saliva.
1850. Luis Pasteur dijo que la fermentación del azúcar en alcohol con levaduras estaba catalizada por “fermentos” que posteriormente se denominaron enzimas.
1897. Años más tarde, Eduard Buchner descubrió que los extractos de la levadura pueden fermentar el azúcar en alcohol fuera de la estructura de las células vivas. Este hecho animó a los bioquímicos a intentar aislar muchas enzimas diferentes y poder examinar sus propiedades.
En 1926, James Summer aisló la ureasa, hecho que impulsó los primeros estudios sobre las propiedades de las enzimas.
Más tarde en los años 30 se cristalizaron las enzimas pepsina y tripsina.
La última parte del siglo y principios del siglo XXI ha habido una investigación más intensa sobre las enzimas que catalizan el metabolismo celular, purificando millares de enzimas que se aplican en muchísimos ámbitos.
Estructura
Como hemos comentado, la mayoría de las enzimas son proteínas, por lo que no requieren más grupos químicos que residuos aminoácidos para su actividad.
En cambio, otras enzimas requieren un componente químico adicional, llamado cofactor.
↳ El cofactor son uno o varios iones inorgánicos como Fe2+, Mg2+, Mn2+ o Zn2+, o un complejo orgánico o metalorgánico denominado coenzima.
Algunas enzimas requieren una coenzima o uno o más iones metálicos para su actividad. Una coenzima unida a la proteína enzimática se denomina grupo prostético.
Cofactores minerales
Comprenden un gran grupo de sustancias inorgánicas con una mayoría de iones metálicos.
Zinc
- Es el más ubicuo y versátil de los cofactores metálicos. Más de 300 enzimas tienen un cofactor de zinc.
- Aproximadamente el 3% del genoma de los mamíferos codifica para proteínas dedos de zinc unidas al ADN.
- También participa en enzimas como la anhidrasa carbónica, la cual es requerida para la secreción del ácido clorhídrico en el estómago, carboxipeptidasa, aspartato-transcarbamilasa y alcohol deshidrogenasa, oligometafosfatasa, entre otras.
- Se absorbe en el duodeno y se fija débilmente a casi todas las proteínas plasmáticas, principalmente a la albúmina. Esto es importante para su transporte hacia los tejidos.
Una vez allí, se acumula débilmente en los tejidos y ante una dieta insuficiente la concentración plasmática baja rápidamente.
Hierro
La mayoría de las enzimas con hierro acoplan el hierro como heme, o como un arreglo especial de hierro con grupos azufre, conocidos como centros hierro-azufre.
→ El citocromo c es una proteína heme común en las mitocondrias donde los ligandos axiales al hierro están ocupados por histidina y metionina.
- Las enzimas con un grupo heme tienen un color rojizo, dependiendo del estado de oxidación del hierro, hecho que motivó a nombrar a las proteínas heme de las mitocondrias como “citocromo”.
- La enzima más conocida es la citrocromo c oxidasa, siendo la enzima capaz de dividir una molécula de oxígeno para formar agua.
→ Las enzimas con centros hierro-azufre serían xantina-oxidasa, succinato deshidrogenasa y nitrogenasa.
Cobre
- El cobre participa en numerosas enzimas, aunque no tan abundante como el Zinc, cumpliendo importantes funciones biológicas principalmente dentro del citosol.
- La mayor parte son oxidasas, y participa junto con el hierro en la citocromo oxidasa.
- Las enzimas de cobre pueden ser simples o complejas dependiendo del número de átomos de cobre que contengan. La dopamina-beta-monooxigenasa contiene 8 átomos de cobre.
- A muchas proteínas el cobre les da un color azul, como a la ceruloplamina.
- Debido a la tendencia a aceptar electrones, el cobre es un poderoso oxidante.
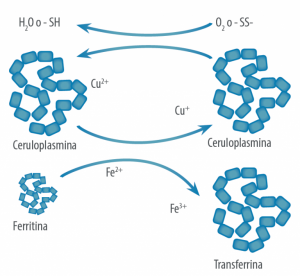
Los sitios cobre de la ceruloplasmina tienen capacidad de oxidar Fe2+ a Fe3+; lo que prepara los iones hierro para unirse a la transferrina, y entregar hierro a órganos y tejidos. Esta reacción liga los dos elementos y podría explicar por qué cuando existen carencias de cobre puede presentarse anemia.
Manganeso
Podría ser el elemento menos común en las enzimas, y a veces también el gran olvidado. Pero el manganeso participa en enzimas importantes como la piruvato-carboxilasa, y la arginasa en el ciclo de la urea.
También actúa como cofactor activador del metal para muchas enzimas que requieren magnesio, como la fructosa 1.6 difosfatasa, galactoquinasa, glucosa 1.6 fosfomutasa, glutatión reductasa y peptidasa, entre otras.
Magnesio
- Es requerido por un gran número de enzimas, entre ellas las fitasas que son de las más utilizadas en alimentación animal.
La carencia de magnesio no permite activar las fitasas, bajando la efectividad de las mismas.
- También participa en otras enzimas, todas muy ligadas al fósforo también como alcalina fosfomonoesterasa, arginina cinasa, aspartasa, ATPasa, decarboxilasa, fosfofructoquinasa, fosforilasa.
- Además, el magnesio está implicado en rutas metabólicas importantescomo la glicólisis con enzimas como la piruvato-quinasa o la hexoquinasa.
Cobalto
- El cobalto como cofactor está muy ligado a la vitamina B12. La forma más habitual de la coenzima que contiene cobalto es la cianocobalamina.
- Participa, pero en menor medida y como cofactor, junto con otros minerales en enzimas como alcalina fosfomonoestarasa, la fenoloxidasa o la trifosfatasa.
Calcio
- El calcio es un cofactor para un número limitado de coenzimas. Las más importantes y relevantes son alfa-amilasa y la termolisina.
- Participa también en el complejo actina-miosina del músculo, pero sus funciones son más importantes en otras vías y rutas metabólicas que como cofactor.
Otros minerales
Existen otros muchos minerales como el molibdeno, el vanadio, la sílice, el selenio y el níquel que participan, en mayor o menor medida, en muchos procesos catalíticos.
Hemos visto que las enzimas son esenciales en los organismos biológicos, siendo importantes catalizadores de muchas rutas. Sin ellas algunos procesos tardarían años en realizarse y gracias a las enzimas en pocos segundos se produce la reacción.
Los minerales, a su vez, son importantes en su justa dosificación porque una carencia ocasiona que las enzimas no puedan activarse y ejercer su función correctamente, pudiendo aparecer enfermedades graves o leves dependiendo de la importancia de la enzima en la ruta metabólica.
En estos últimos años, la aparición de enzimas exógenas que podemos aditivar a los piensos para mejorar los crecimientos, optimizar nutrientes, y por tanto, bajar el coste ha sido muy importante.
Aun así, no podemos descuidar que a nivel interno existen más de 10.000 enzimas que son necesarias para el correcto funcionamiento de todos los procesos biológicos, y estas enzimas no pueden funcionar correctamente si sus activadores no están presentes.
Por ello, es necesario formular y proporcionar a los animales los minerales, macro y micro, en la dosificación que corresponda para que las enzimas puedan desarrollar toda su actividad.
Autor: Toni Adsuara Martínez – Quimialmel, S.A.
Artículo publicado en: www.nutricionanimal.info – Revista Nutrinews





Deje su comentario